生物医药和创新药是当前医药领域的重要关键词。生物医药行业利用生物技术和医学知识,致力于研发和生产用于预防、治疗和诊断疾病的药物和医疗器械。创新药则是指具有新的治疗机制和疗效的药物,能够满足患者需求并改善临床疗效。生物医药和创新药的发展对人类健康具有重要意义,它们能够提供更安全、有效的治疗方案,并推动医学的进步。然而,生物医药和创新药的研发面临着诸多挑战,如高成本、临床试验的复杂性等。因此,需要加强科研合作和创新,加大对生物医药和创新药的支持力度,为科学家和企业提供更好的发展环境,以推动生物医药和创新药的健康发展,造福人类健康。
近日,“中国毒理学会药物毒理与安全性评价学术大会(2023年)暨粤港澳大湾区生物医药产业第二届高峰论坛”在中国深圳坪山成功举办。
本次大会主席廖明阳研究员致开幕词时表示,会议旨在推动我国生物医药产业的发展,把控“粤港澳大湾区”和广大生物医药产业利好政策,提升创新药物安全性评价研究工作,特别是抗体药物、细胞和基因治疗药物的安全性评价研究水平,实现国内创新药物非临床安全性评价在技术水平和规范与国际接轨,搭建药物毒理学研究的最新进展和药物临床前安全性评价新思路、新技术和安全性评价国际政策以及医药产业的高端学术交流平台。
中国新药临床试验次数。据前瞻产业研究院数据显示,2016年以来,中国新药临床试验数量持续增长,尤其是2019年以来,新药临床试验数量较以前年度有较大的突破,连续三年超过800个,2021年超过1400个,同比增长47.96%。
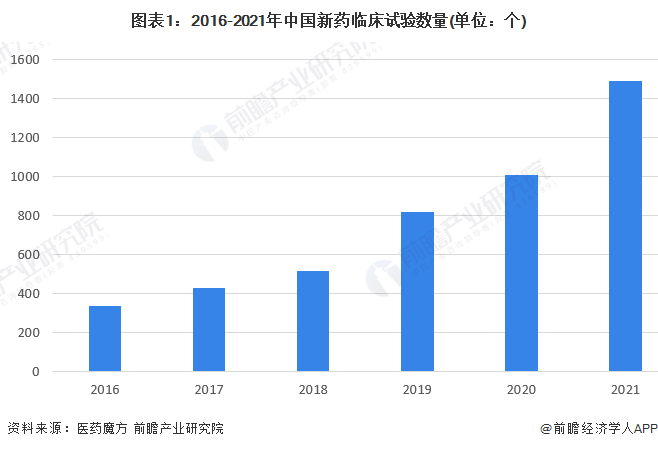
中国创新药获批类型。2016年以来,中国创新药获批数量波动上升,2021年达到89款。从中国创新药获批类型看,化学药数量最多,2016年以来共计234款,其次是生物药共计114款,中药获批数量较少仅为24款。

中国首次IND药品数量分析。2012-2019年间,我国首次IND药品数量整体呈波动递增趋势增长;2020年受新型冠状病毒肺炎疫情影响,我国首次IND药品数量激增,总数由2019年的298款增长至2020年的441款,2021年中国首次IND药品数量再创历史新高,达到644款,两年分别同比增长47.99%和46.03%;国产药物方面,国产药物IND数量自2017年开始显著增长,2017年国产药物IND数量达189款,同比增长112.36%;2019-2021年国产药物IND数量占比一路增长,由2019年的62.75%增长至2021年的76.09%。
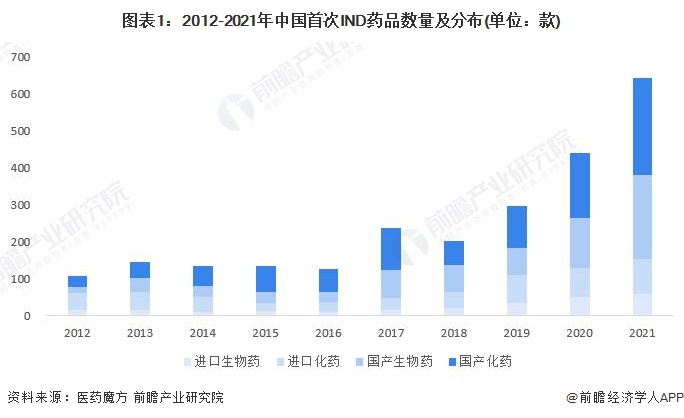
我国创新药研发趋势。虽然我国目前创新药的研发水平距离全球领先国家仍有一定差距,但未来,鉴于我国医药外包行业在全球的领先地位,以及庞大的市场。我国有实力成为全球药物创新中心;且随着中国新冠疫苗在全球普及程度提高,国家规划对生物医药的高度重视,我国生物医药行业在创新药研发方面未来可期。

国家药监局药品注册管理司药物研究处一级调研员叶国庆女士表示,国家药监局从2014年开始深化药品审批制度改革,促进创新药上市,旨在保障群众的用药安全。其中一项重要工作就是制定药物非临床研究质量管理规范并监督执行。
国家药品监督管理局药品审评中心药理毒理部副部长黄芳华研究员表示,安全、有效、质量可控是药品的三大属性。“安全性问题”永远是创新药物中重点关注的问题,,是影响创新医药产业发展的重要支撑点问题。
广东省药品监督管理局党组成员、副局长方维表示,随着我国药物医疗器械审评审批制度的改革,新时代安全性评价研究领域的热点和难点都发生变化,安全性评价也将与时俱进。突如其来新冠疫情对生物医药产业发展提出了新要求,也凸显了生物医药产业在提高人民生命健康质量中的重要价值。
前瞻经济学人APP资讯组
更多本行业研究分析详见前瞻产业研究院《中国生物医药行业发展前景预测与投资战略规划分析报告》。
同时前瞻产业研究院还提供产业大数据、产业研究报告、产业规划、园区规划、产业招商、产业图谱、智慧招商系统、IPO募投可研、IPO业务与技术撰写、IPO工作底稿咨询等解决方案。
未经允许不得转载:零时古怪 - 中国第一时事资讯综合门户 » 黄芳华研究员:“安全性问题”永远是创新药物中重点关注的问题【附创新药行业分析】

 零时古怪 - 中国第一时事资讯综合门户
零时古怪 - 中国第一时事资讯综合门户









